Escolares, adolescentes y adultos (≥ 6 años)
Cuadro
sinóptico 3.2
En pacientes de ≥ 6 años de edad sugerimos que la sospecha clínica de
asma esté basada en la presencia de dos o más de los síntomas clave: sibilancias,
tos, disnea y opresión del pecho o sensación de pecho apretado.
La tos generalmente es paroxística y de predominio nocturno. La
ausencia de sibilancias no descarta el asma. Una característica del asma es la
variabilidad de los síntomas, que fluctúan en intensidad y frecuencia, incluso
en un mismo día.
Así que es más probable que sea asma si los síntomas van y vienen con
el tiempo; por ejemplo, si empeoran en la noche, en la madrugada o al
despertar; si son desencadenados por factores como son ejercicio, reír,
exposición a alérgenos o aire frío y/o si empeoran durante infecciones virales.
En algunos pacientes pueden desencadenarse con la ingesta de antiinflamatorios
no esteroideos (AINES) o betabloqueadores. Ninguno de estos síntomas y signos
es específico para el asma, pero la historia familiar o personal de enfermedad
alérgica (dermatitis atópica, rinitis alérgica, asma alérgica) aumenta la
predisposición o la gravedad del asma.
Aparte de la atopia existen otros detalles de la historia clínica
personal o familiar que pueden aumentar o reducir la probabilidad de que sea
asma, tabla
3.1.
Sospecha de asma en lactantes y
preescolares (≤ 5 años)
Cuadro
sinóptico 3.3
En pacientes menores de 5 años el diagnóstico de asma es complejo,
porque los síntomas respiratorios (tos y sibilancias episódicas) son comunes
durante infecciones respiratorias virales.
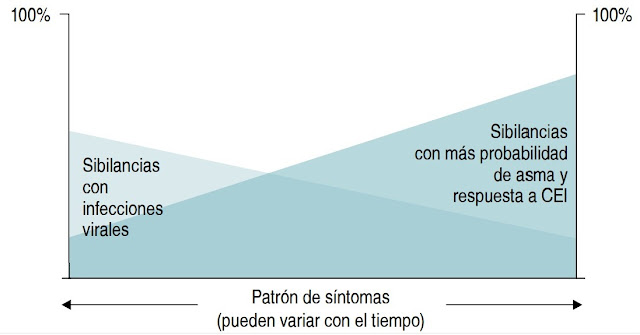
En niños < 5 años: Probabilidad de diagnóstico de asma y respuesta
a corticoesteroides inhalados (CEI)
En niños < 5 años:
probabilidad de diagnóstico de asma y respuesta favorable a corticoesteroides
inhalados (CEI). Adaptado de: GINA 2016.
Además, no existen pruebas de
rutina para documentar una limitación del flujo de aire. En ciertos niños
llamados «sibilantes tempranos transitorios», la tendencia a la recurrencia de
las sibilancias con infecciones puede provocar confusión diagnóstica,
particularmente antes de los 2 años. En estos niños con sibilancias el conjunto
de ciertos datos clínicos puede aumentar la probabilidad de que desarrolle asma
en un futuro, vea parte derecha de figura 3.1. Es más probable que estos niños
respondan favorablemente al tratamiento con corticoesteroides inhalados (CEI),
Al igual que en niños mayores, sugerimos que la sospecha clínica de asma en
niños ≤ 5 años se base en la presencia de forma periódica o recurrente de dos o
más de los síntomas respiratorios clave, variando con el tiempo en intensidad y
frecuencia: 1. Sibilancias. 2. Tos. 3. Dificultad respiratoria. 4. Opresión del
pecho o sensación de pecho apretado. Si estos cuatro síntomas en niños
presentan ciertas características, hacen el diagnóstico de asma más probable
(tabla 3.2). En algunas ocasiones la tos persistente como único síntoma, de
predominio nocturno/en la madrugada y/o al despertar y/o con ejercicio, puede
ser considerado como una variante de asma en el niño pequeño. Estudios de
cohorte, con seguimiento desde el nacimiento, han permitido el desarrollo de
algunas herramientas para predecir el riesgo de padecer asma en los niños con
sibilancias durante los primeros años de vida. El más conocido es el Índice
Predictivo de Asma (por sus siglas en inglés API,7 desarrollado a partir de los
datos de niños del estudio de cohorte de Tucson.8,9 Empero, estos instrumentos
basados en puntaje obtenido en función de la presencia de determinados factores
tienen valores predictivos modestos (valor predictivo positivo 77%, valor
predictivo negativo 68%, especificidad 97%), por lo que carecen de la precisión
suficiente para hacer pronósticos fiables. Con esta reserva y ante la falta de
otros instrumentos más precisos, sugerimos su uso cuando sea necesario, pero se
recomienda interpretar sus resultados con cautela (figura 3.2).

El índice predictivo del asma
indica la probabilidad de que el paciente con sibilancias tempranas desarrolle
asma persistente en un futuro. Aquí presentamos su versión modificada con mejor
valor predictivo positivo y negativo. Adaptado de referencia 9.
Obstrucción al flujo de aire: espirometría
Cuadro sinóptico 3.4
El asma es una enfermedad en la
cual la función pulmonar está afectada. Las dos maneras más utilizadas para
determinar el flujo de aire son la espirometría forzada y la flujometría.

En pacientes con un cuadro
clínico sugestivo de asma, se recomienda la espirometría como la prueba de
primera elección para demostrar obstrucción al flujo de aire espiratorio,
sobretodo en niños ≥ 6 años y adultos. Normalmente una persona logra exhalar >
80% de la capacidad vital forzada (FVC) dentro de un segundo (que es el FEV1).
Así que la relación FEV1/FVC debajo del 70% en adultos menores de 50 años es
diagnóstico de obstrucción al flujo de aire. La gravedad de la obstrucción la
indica el valor de FEV1 en relación al valor predicho: arriba de 70% es una
obstrucción leve y 60-69% una obstrucción moderada. Este porcentaje se reporta
automáticamente en el resultado de la espirometría. Expertos del Instituto
Nacional de Enfermedades Respiratorias (INER) recientemente hicieron una
revisión de la técnica exacta de la espirometría (figura 3.3). 10 Sólo en
situaciones sin acceso a un espirómetro se puede usar la flujometría para
documentar obstrucción, sin embargo, su resultado es altamente variable. En la
actualidad, existen espirómetros para uso individual por parte de los
pacientes. El desempeño técnico de estos dispositivos para monitoreo del FEV1
es ampliamente confiable con fines de diagnóstico y de seguimiento. Aunque no
se menciona en las guías madre, GUIMA lo anota como punto de buena práctica.(3)
Dado el carácter fluctuante del proceso obstructivo, un resultado de
espirometría normal en un paciente con una historia y síntomas sugestivos de
asma no descarta la enfermedad. En pacientes con grados leves (intermitente y
persistente) de asma, en muchas ocasiones la espirometría puede ser normal. A
veces se logra finalmente demostrar el patrón obstructivo fluctuante con
pruebas seriadas de función pulmonar. Por ello, si el diagnóstico es muy
probable, sugerimos iniciar el tratamiento del asma aún con una espirometría
normal, vea 3.6. En pacientes con un diagnóstico probable o poco probable de
asma, sugerimos intentar demostrar variabilidad en la obstrucción al flujo de
aire con las pruebas de reversibilidad y la prueba de reto, abajo descritas.

Ejemplos de curvas de la
espirometría características del paciente con asma. Curvas volumen-tiempo
(izquierda) y flujo-volumen (derecha) de una espirometría. Con asma el aumento
de volumen en el tiempo es más lento y el máximo del flujo más bajo y corto.
Esto mejora (parcialmente) en la prueba pos broncodilatadora.
Nota: Pacientes con asma leve
persistente generalmente no presentan alteración alguna en la espirometría.
Neumol Cir Torax, Vol. 76, Suplemento 1, 2017